Vor zwanzig Jahren haben neue Präzisionsarzneimittel die Art, wie wir Krebs behandeln, verändert, indem sie auf die spezifischen Proteine mit Fehlfunktionen abzielten, die die individuelle Krankheit eines Patienten auslösen. Doch Krebs ist eine komplexe Krankheit. Wissenschaftler, die daran arbeiteten, diesen Ansatz so umfassend wie möglich anzuwenden, sahen sich – neben vielen anderen – vor allem mit einer Herausforderung konfrontiert: Die meisten der bekannten krebsauslösenden Proteine galten als "nicht behandelbar".
Was kann also getan werden? Eine Möglichkeit könnte darin bestehen, der Zelle zu helfen, ihren Müll zu entsorgen.
Was bedeutet "nicht behandelbar" überhaupt?
Das Ziel von Krebsmedikamenten ist es, kranke Zellen daran zu hindern, unkontrolliert zu wachsen, während normale Zellen so gesund wie möglich erhalten werden.
Da fehlerhafte Proteine ein unkontrolliertes Zellwachstum verursachen, besteht eine wichtige Strategie darin, diese Proteine an ihrer Arbeit zu hindern. Um dies zu erreichen, können Wissenschaftler aktivitätshemmende Medikamente entwickeln, die an ganz bestimmte Stellen eines in Frage kommenden Proteins binden – wie ein Schlüssel, der nur in ein bestimmtes Schlüsselloch passt.
Viele Proteine - darunter eine Familie von sogenannten Transkriptionsfaktoren, die zu den am häufigsten mutierten Proteinen bei Krebs gehören - haben jedoch von vornherein nicht die nötigen Eigenschaften, die sie für die Behandlung mittels zielgerichteter Medikamente im Sinne der klassischen medizinischen Chemie qualifizieren. Im Grunde genommen sind diese Proteine "nicht behandelbar", weil ihnen ein Schlüsselloch fehlt.
Präzise Kehrichtbeseitigung
Aus dem Biologieunterricht in der Schule kennen viele von uns sicherlich noch die Analogie zwischen einer Zelle und einer Stadt; mit Strassen, Kraftwerken, Lagerhäusern und vielem mehr. Doch damit nicht genug: Zellen verfügen sogar über ein Kehrichtentsorgungssystem – speziell für Proteine.
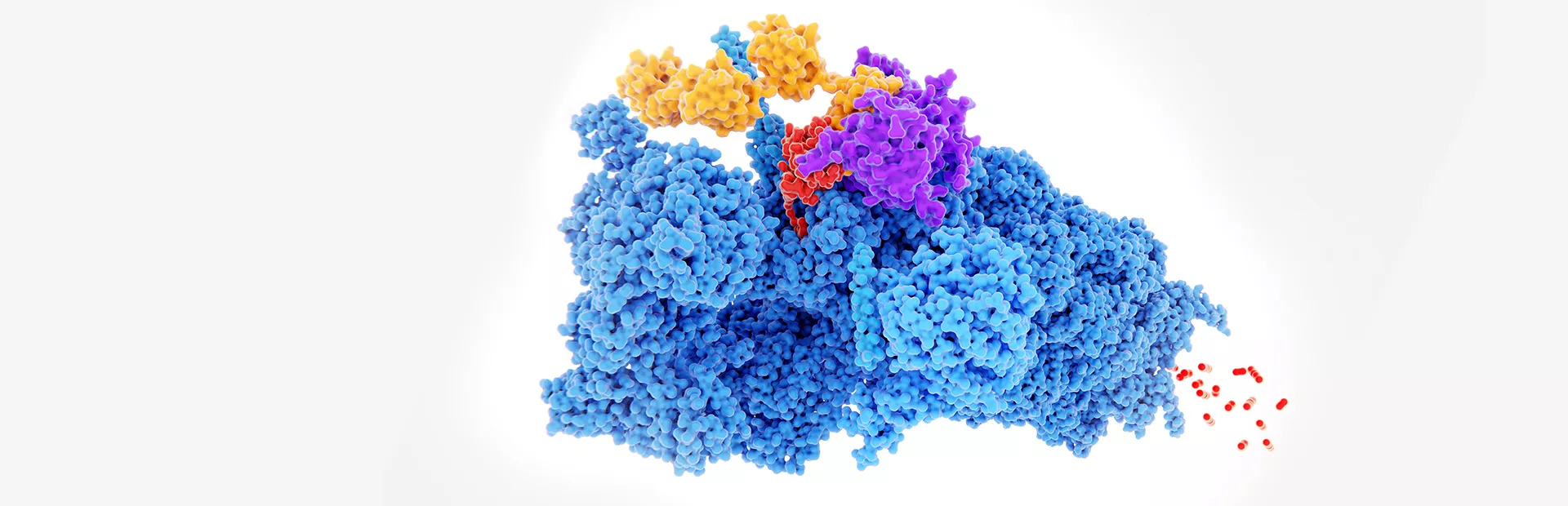
Dabei handelt es sich um eine zelluläre Maschine namens Proteasom, eine Art Kehrichtabfuhr, die durch die Zelle fährt und alte, unerwünschte oder kaputte Proteine abbaut. Hierbei erkennt das Proteasom jene Proteine, die abgebaut werden sollen, anhand einer chemischen Markierung namens Ubiquitin, die von anderen spezialisierten molekularen Maschinen an Proteinen angebracht wird.
Wenn Wissenschaftler herausfinden können, wie man ein Zielprotein auf die richtige Weise mit Ubiquitin markiert, könnte dies die Tür für neue potenzielle Therapien öffnen. Mit diesem Ansatz, der als gezielter Proteinabbau (engl. targeted protein degradation, TPD) bezeichnet wird, könnte nicht nur die Aktivität eines ausser Kontrolle geratenen Proteins gehemmt; man könnte unter Umständen das Protein als Ganzes aus der Zelle entfernen. Dies schliesst die eingangs genannten, "nicht therapierbaren" Proteine ein. Salopp formuliert: Anstatt nur nach dem richtigen Schlüsselloch für ein krebserregendes Protein zu suchen, könnte man also versuchen, das ganze Ding in den Kehricht zu werfen.
Der gezielte Proteinabbau befindet sich noch in einem sehr frühen Stadium, und Wissenschaftler von Novartis arbeiten hart daran, sein Potenzial für die Patienten zu nutzen. Mit Hilfsmitteln wie molekularen Klebstoffen versucht man, die Ubiquitin-Markierungsmaschinerie der Zelle dazu zu bringen, mit den Zielproteinen zu interagieren, sodass das Proteasom sie abbauen kann.
Dabei ist dieser Vorgang nicht auf Proteine in Krebszellen beschränkt - der gezielte Proteinabbau könnte potenziell "nicht therapierbare" Proteine in anderen Zellen kontrollieren, z. B. in bestimmten T-Zellen, um die Ergebnisse der Immuntherapie zu verbessern.