Von Elizabeth Dougherty
Zellen in allen Lebewesen haben eine eingebaute Such- und Löschfunktion. Die Existenz eines solchen Mechanismus war bis vor rund 30 Jahren unbekannt – bis zu dem Tag, an dem Forscher, die mit Petunien experimentierten, ihn zufällig entdeckten. Heute jedoch wollen Wissenschaftler diese Eigenschaft in der Medizin nutzen.
Medikamente, die sich dieses Such- und Löschmechanismus bedienen, sollen die Produktion krankheitsrelevanter Proteine blockieren, indem sie die RNA ins Visier nehmen, also auf die zellinterne Maschinerie, nach deren Anweisungen die Zellen normalerweise Proteine aufbauen. Diese neue Art von Therapeutika hat das Potenzial, fast jeden Krankheitsprozess im Körper zu unterbrechen. Novartis entwickelt beispielsweise innovative experimentelle Therapien, die sich auf die RNA fokussieren und die das Potenzial haben, den Cholesterinspiegel zu senken und das Risiko von traumatischen Ereignissen im Zusammenhang mit Herzerkrankungen wie Herzinfarkten oder Schlaganfall zu reduzieren.
In diesem Artikel nehmen wir Sie mit auf einen visuellen Rundgang durch die Geschichte der RNA-gerichteten Medikamente von 1990 bis heute.
Das Problem mit den violetten Petunien

1990 wollte ein Wissenschaftler an der Universität von Arizona violette Petunien noch violetter machen. Sein Team fügte der Pflanze Gene hinzu, die für die Farbe Violett kodierten, und wartete, bis die Blumen blühten. Doch der Plan ging schief: Anstelle von sattem Violett erstrahlten die Petunien in schönstem Weiss.
Die Anweisungen für violette Pigmente, die die Forscher in die Pflanze eingebracht hatten, hatten versehentlich - und auf mysteriöse Weise - die natürlich vorkommenden violetten Anweisungen der Blume blockiert, ohne die DNA der Blume zu verändern. Heute wird dieser Mechanismus als RNA-Interferenz bezeichnet; er ist einer von zwei möglichen Wegen, um die Produktion von Proteinen zu stören, indem man auf deren RNA abzielt. Diese Möglichkeiten waren 1990 jedoch noch unbekannt - alles, was die Wissenschaftler hatten, war ein fehlgeschlagenes Experiment und ein Haufen weisser Petunien.
Vom Mysterium zum nützlichen Werkzeug

Das Petunien-Experiment spornte Wissenschaftler auf der ganzen Welt an, mehr erfahren zu wollen. Ein Team unter der Leitung der Wissenschaftler Craig Mello und Andrew Fire experimentierte mit zielgerichteter RNA in winzigen Würmern namens C. elegans.
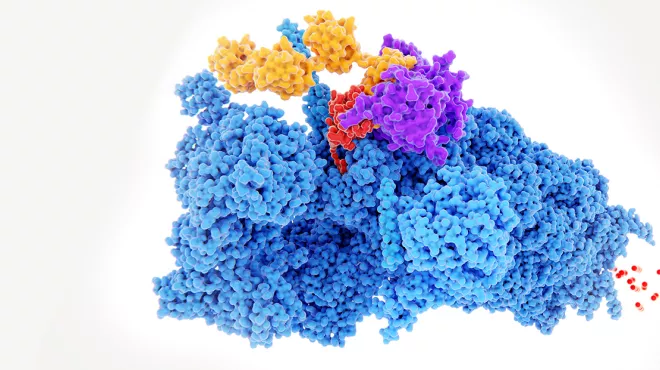
Mello und Fire konstruierten einen RNA-Doppelstrang, der aus Nukleinsäuren, den Bausteinen von DNA und RNA, besteht. Das Muster des Strangs aus Nukleinsäuren passte zu den RNA-Anweisungen für ein Muskelprotein, das von den Würmern produziert wird. Als sie den Strang in die Würmer injizierten, löschte er die passenden RNA-Anweisungen in den Zellen der Würmer aus.
Es war, als hätten sie den Ziel-RNA-Code in das Such- und Löschfeld eines Textverarbeitungsprogramms eingegeben und "Enter" gedrückt. Die Würmer hörten auf, das Muskelprotein zu produzieren und begannen zu zucken, eine bekannte Nebenwirkung eines Mangels an diesem Protein.
Indem man diesen Mechanismus nachahmt, könnten die Forscher potenziell die Produktion fast aller Proteine stören, einschliesslich derer, die an Krankheiten beteiligt sind. Aufgrund des Potenzials dieser Entdeckung, die Medizin nachhaltig zu verändern, erhielten Mello und Fire 2006 den Nobelpreis für Physiologie oder Medizin.
Heute gibt es mehrere zugelassene Medikamente, die auf RNA basieren. Diese Medikamente wirken auf unterschiedliche Weise: Einige Medikamente bedienen sich sogenannter "small interfering RNA", andere wiederum verwenden einzelne RNA-Stränge, sogenannte Antisense-Oligonukleotide, um ein krankheitsrelevantes Protein zu suchen und zu löschen. Darüber hinaus verwenden einige COVID-19-Impfstoffe die sogenannte Boten-RNA (engl. messenger RNA, kurz mRNA), um das Immunsystem darauf zu trainieren, virale Proteine zu erkennen und körpereigene Schutzmassnahmen einzuleiten.
Die perfekte Verkleidung

Die Fähigkeit, RNA-Instruktionen zu suchen und zu löschen, wird seither in Labors zu Forschungszwecken genutzt, aber seit den Entdeckungen von Mello und Fire sollten noch knapp 20 Jahre vergehen, bis das Versprechen von RNA-targeting auch in der Medikamentenentwicklung in den Fokus rückte.
Eine der Herausforderungen bestand darin, dass die Nukleinsäuren, aus denen RNA-gerichtete Medikamente bestehen, viralen Eindringlingen sehr ähnlichsehen. Wenn diese Stränge im Körper zirkulieren, wehrt sich das menschliche Immunsystem mit einer Abwehrreaktion.
Damit RNA-gerichtete Medikamente wirken können, müssen sie durch den Körper fliessen und unbemerkt an ihr zelluläres Ziel gelangen. Also haben sich Wissenschaftler clevere Verkleidungen ausgedacht, die wie ein Tarnmantel funktionieren: Ein zusätzliches Atom hier und eine winzige chemische Veränderung dort können verhindern, dass das RNA-gerichtete Medikament vom Immunsystem entdeckt wird.
Eine neue Art von Medizin

RNA-Targeting-Medikamente enthalten manchmal sowohl den getarnten Suchstrang als auch ein kleines Molekül, das den Strang wie ein Navigationsgerät zu einer Zielzelle leitet. Der Leitfaden stellt sicher, dass die gezielten RNA-Anweisungen nur in den richtigen Zellen gelöscht werden, etwa in einer Krebszelle oder in einer Zelle, die ein krankheitsförderndes Protein produziert.
Sobald das Medikament die richtige Zelle gefunden hat, dringt es in sie ein und installiert sich – vergleichbar mit einer App, die auf unseren Smartphones im Hintergrund läuft. Das getarnte und präzise gesteuerte RNA-Targeting-Medikament kann monatelang ohne Unterbrechung seine Arbeit verrichten und wiederholt RNA-Anweisungen löschen.
RNA-Targeting-Medikamente werden in der Regel als Injektionen formuliert. Da einige von ihnen monatelang aktiv bleiben können, können diese Injektionen potenziell seltener verabreicht werden. Dies macht sie zu einer neuen Art von Medikamenten, sowohl in Bezug auf die klinische Praxis als auch aus biologischer Perspektive.