NU DISPERA
Novartis România: Reimaginăm medicina în continuare.
Terapiile personalizate în cancerele hematologice devin o rutină la nivel mondial.
Introducerea terapiilor cu celule CAR-T în România reprezintă un pas uriaș în tratamentul neoplasmelor hematologice refractare la orice alt tip de tratament, iar Novartis este lider în acest domeniu.
Marcelo Rainer, Novartis România
Ne puteți spune care este misiunea globală a Novartis în ceea ce privește asistența medicală?
Novartis reimaginează medicina pentru a îmbunătăți și prelungi viața oamenilor. În calitate de lider mondial în domeniul medicamentelor, folosim știința inovatoare și tehnologiile digitale pentru a crea tratamente transformatoare în domenii de mare nevoie din punct de vedere medical. Astfel, ne clasăm în mod constant printre cele mai importante companii din lume care investesc în cercetare și dezvoltare. Produsele Novartis ajung la aproape 800 de milioane de oameni la nivel global și găsim modalități inovatoare de a extinde accesul la cele mai recente tratamente ale noastre pentru toți cei care au nevoie de ele.
Care sunt principalele inovații Novartis în hematologie și oncologie la nivel mondial?
Novartis se concentrează pe știință, căutând să transforme vieți și depunând eforturi pentru a găsi tratamente pentru pacienți. În urmă cu mai bine de 20 de ani, Novartis a primit aprobarea din partea US Food and Drug Administration pentru prima terapie țintită pentru cancer, cunoscută sub numele de inhibitor de tirozin kinază, transformând peisajul tratamentului pentru leucemia mieloidă cronică și deschizând ușa pentru a reimagina posibilitățile pentru alte forme de cancer și afecțiuni ale sângelui. La vremea respectivă, revista Times Magazine a citat pe coperta din mai 2001: "Există o nouă muniție împotriva cancerului - acestea sunt gloanțele". Terapia Novartis a fost considerată o "descoperire - nu numai pentru ceea ce face, ci, mai important, pentru strategia revoluționară pe care o reprezintă".

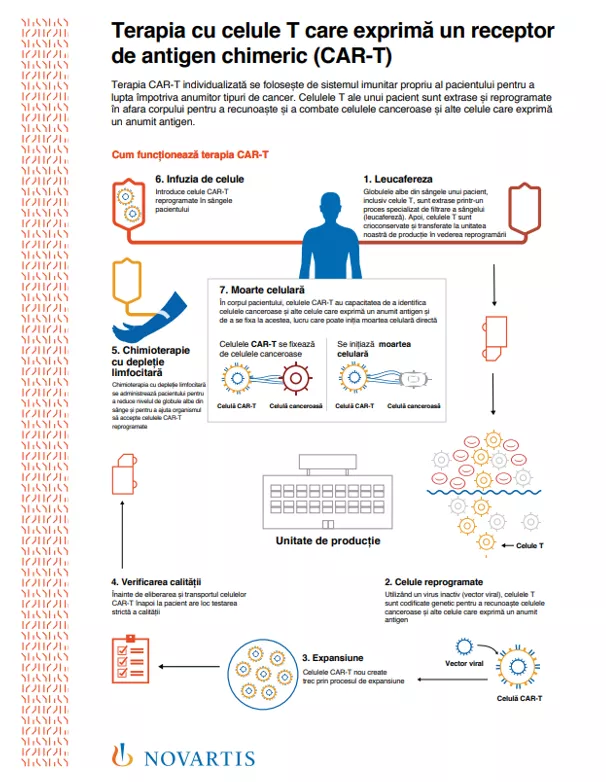
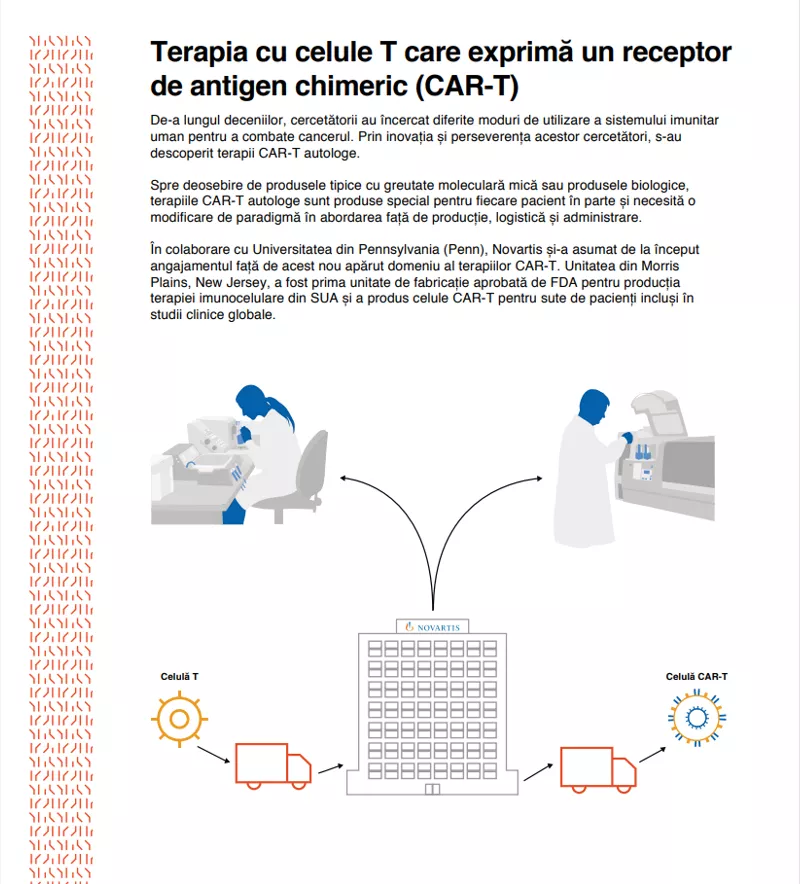
În prezent, Novartis este pionier în clasa tratamentelor celulare și genice și a dezvoltat prima terapie celulară CAR-T aprobată pentru pacienții pediatrici și adulți tineri cu leucemie acută limfoblastică cu celule B recidivantă/refractară și pentru adulții care suferă de limfom difuz cu celulă mare de tip B recidivant/refractar. Această moștenire include stabilirea standardului în ceea ce privește sprijinul acordat pacienților și îngrijitorilor, siguranța și eficacitatea, accesul și parteneriatele cu instituțiile de sănătate, autoritățile locale de sănătate și instituțiile academice din întreaga lume.
Există alte terapii inovatoare Novartis care se află acum în faza de aprobare în Europa sau în România?
Prin activitatea noastră principală - descoperirea, dezvoltarea și comercializarea de tratamente inovatoare - am contribuit la prevenirea și tratarea bolilor, la ameliorarea suferinței și la îmbunătățirea calității vieții oamenilor din întreaga lume. Dar, pe măsură ce dimensiunea și complexitatea provocărilor din domeniul sănătății la nivel mondial cresc, trebuie să ne lărgim domeniul de acțiune, extinzându-ne și mai mult impactul.
În cadrul Novartis, lucrăm la 4 abordări terapeutice majore pentru tratamentul cancerului: terapia țintită, terapia cu radio liganzi, terapia celulară și genică și imunoterapia, cu rezultate care vor îmbunătăți rezultatele pentru pacienții cu cancer de prostată, sindrom mielodisplazic cu risc crescut, limfom folicular, melanoame mutante și anumite forme de cancere pulmonare.
Cancerul de sân continuă să rămână în centrul atenției, echipa Novartis perseverând în dezvoltarea unor noi terapii personalizate. În timp ce cercetătorii noștri urmăresc neîncetat să dezvolte noi medicamente revoluționare, este de datoria noastră să le aducem pacienților, să creăm parteneriate la nivel local, să creăm acces prin mecanisme de rambursare.
Există în România suficiente centre de expertiză unde se pot administra astfel de terapii? Intenționați să deschideți și alte centre similare pentru bolnavii de cancer?
Terapia celulară CAR-T este o terapie individualizată de ultimă generație, concepută special pentru fiecare pacient. Un centru este deja funcțional în București, la Institutul Clinic Fundeni, și lucrăm îndeaproape cu profesioniștii din domeniul sănătății și cu toți cei implicați, pentru a permite ca noi centre să fie disponibile pentru pacienți, în toată țara. Scopul este de a ne asigura că toți pacienții care pot beneficia de acest tip de tratament ajung la el în timp util și în mod eficient.
Cum intenționați să continuați să reimaginați medicină în România?
Ne-am angajat să punem medicamentele noastre la dispozitia tuturor celor care au nevoie de ele în România. Pentru toate produsele noastre noi, integrăm în mod sistematic strategii de acces în modul în care cercetăm, dezvoltăm și livrăm produsele noastre. Acesta este motivul pentru care în România am construit parteneriate permanente cu profesioniștii din domeniul sănătății, autoritățile, organismele științifice și asociatiile de pacienți, pentru a permite accesul fiecărui pacient adecvat la tratamentele Novartis de care are nevoie. Mai mult decât atât, raportat la numărul de studii clinice inițiate în ultimul deceniu în țara noastră, Grupul Novartis se află în topul companiilor care investesc în cercetare și dezvoltare la nivel local. Viziunea noastră este de a deveni cel mai apreciat și de încredere partener pentru sistemul de sănătate, profesioniștii din domeniul sănătății și pacienți.