Szanowni Państwo,
Podmiot odpowiedzialny Novartis Europharm Limited w porozumieniu z Europejską AgencjąLeków oraz Urzędem Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych i Głównym Inspektoratem Farmaceutycznym pragnie przekazać Państwu następujące informacje
Podsumowanie
- Firma Novartis otrzymała niewielką liczbę zgłoszeń dotyczących trudności z przesunięciem tłoka strzykawki uniemożliwiających wstrzyknięcie produktu leczniczego Leqvio. Problem występuje rzadko na terenie Unii Europejskiej (~ 0,01%).
- Aby zapewnić pacjentom i fachowym pracownikom ochrony zdrowia optymalne korzystanie z produktu leczniczego Leqvio, w czasie, gdy prowadzone są badania techniczne mające na celu rozwiązanie problemu, firma Novartis chce przekazać Państwu ważną informację odnoszącą się do sposobu postępowania przed wstrzyknięciem produktu leczniczego Leqvio:
- Nie należy zdejmować nasadki na igłę do chwili wykonania wstrzyknięcia, ponieważ w rzadkich przypadkach zbyt wczesne zdjęcie nasadki na igłę przed wykonaniem wstrzyknięcia może spowodować zaschnięcie produktu leczniczego wewnątrz igły, co może spowodować brak drożności.
- Jeśli po wkłuciu igły nie będzie można opuścić tłoka, należy użyć nowej ampułko-strzykawki. Firma Novartis dokona reklamacji każdej zablokowanej strzykawki z produktem leczniczym Leqvio. Wskazówki
dotyczące reklamacji produktu zawarte są w Załączniku 1 do niniejszego komunikatu. - Ocena danych potwierdza, że nie występuje żadne klinicznie istotne ryzyko dla bezpieczeństwa pacjentów.
Podstawowe informacje – Wskazówki w drukach informacyjnych produktu
Produkt leczniczy Leqvio jest wskazany do stosowania u osób dorosłych z pierwotną hipercholesterolemią (heterozygotyczną hipercholesterolemią rodzinną i hipercholesterolemią wielogenową) lub dyslipidemią mieszaną, jako uzupełnienie diety:
- w skojarzeniu ze statyną lub statyną wraz z innymi lekami zmniejszającymi stężenie lipidów u pacjentów, u których nie można osiągnąć stężenia LDL-C będącego celem terapii w wyniku stosowania maksymalnej tolerowanej dawki statyny lub
- samodzielnie bądź w skojarzeniu z innymi lekami zmniejszającymi stężenie lipidów u pacjentów nietolerujących statyn lub u pacjentów, u których stosowanie statyn jest przeciwwskazane.
Zalecana dawka to 284 mg inklisiranu w pojedynczym wstrzyknięciu podskórnym podawanym: po raz pierwszy, ponownie po 3 miesiącach, a następnie co 6 miesięcy.
Produkt leczniczy Leqvio jest dostępny w Unii Europejskiej w dwóch postaciach. Obie są przeznaczone do podawania wyłącznie przez osobę z fachowego personelu ochrony zdrowia:
- „ampułko-strzykawka” (bez osłony zabezpieczającej igłę), która nie zawiera dołączonej instrukcji używania oraz
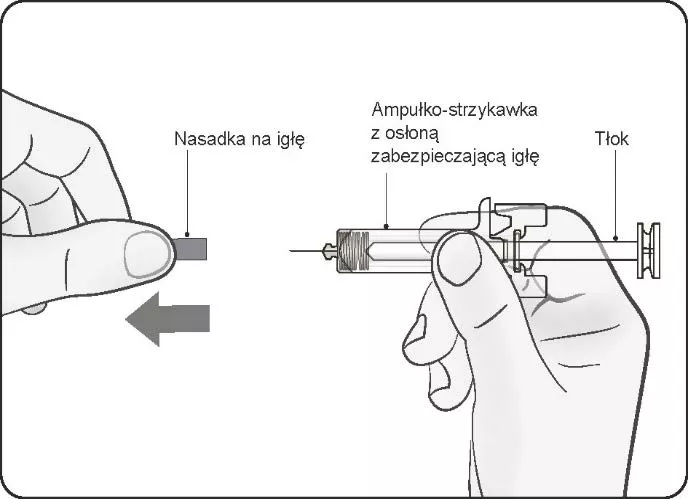
- „ampułko-strzykawka z osłoną zabezpieczającą igłę”, do której dołączono instrukcję używania ze szczegółowymi wskazówkami procedury wstrzyknięcia, w tym aktywacji mechanizmu bezpieczeństwa i instrukcją, by nie zdejmować nasadki na igłę do chwili wykonania wstrzyknięcia.
Firma Novartis pragnie podkreślić ważną informację dotyczącą kroku przed wstrzyknięciem produktu leczniczego Leqvio:
- Nie należy zdejmować nasadki na igłę do chwili wykonania wstrzyknięcia.
Ta ważna informacja znajduje się obecnie w instrukcji używania produktu Leqvio w ampułkostrzykawce z osłoną zabezpieczającą igłę. Firma Novartis wprowadzi instrukcję używania dla produktu leczniczego Leqvio w postaci ampułko-strzykawki (bez osłony zabezpieczającej igłę), aby przekazać tę ważną wskazówkę konsekwentnie dla obu postaci leku.
Ampułko-strzykawka „bez” osłony zabezpieczającej igłę | Ampułko-strzykawka „z” osłoną zabezpieczającą igłę |
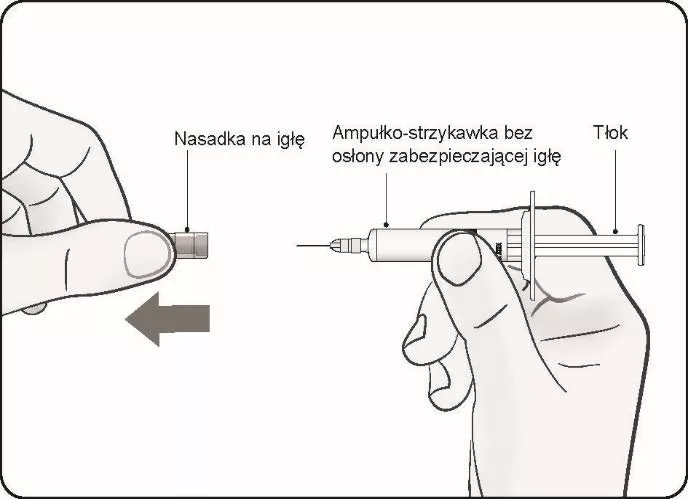
| 
|
Należy także pamiętać, że:
- Jeśli po wkłuciu igły nie można opuścić tłoka, należy użyć nowej ampułkostrzykawki.Firma Novartis dokona reklamacji każdej zablokowanej strzykawki z produktem leczniczym Leqvio. Wskazówki dotyczące reklamacji produktu zawarte są w Załączniku 1 do niniejszego komunikatu.
- Ocena danych potwierdza, że nie występuje żadne klinicznie istotne ryzyko dla bezpieczeństwa pacjentów.
Zgłaszanie działań niepożądanych
Fachowi pracownicy ochrony zdrowia powinni zgłaszać wszelkie podejrzewane działania niepożądane związane ze stosowaniem produktu leczniczego Leqvio za pośrednictwem Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych:
al. Jerozolimskie 181C, 02-222 Warszawa
tel.: + 48 22 49 21 301
faks: +48 22 49 21 309
Strona internetowa: https://smz2.ezdrowie.gov.pl
lub do przedstawiciela podmiotu odpowiedzialnego - firmy Novartis korzystając z następujących danych kontaktowych:
Novartis Poland Sp. z o.o.
ul. Marynarska 15
02-674 Warszawa
Dział ds. Bezpieczeństwa Pacjentów
tel: +48 22 375 48 80
faks: +48 22 375 47 50
e-mail: zdarzenia.niepozadane@novartis.com
Dane kontaktowe firmy
Novartis Poland Sp. z o.o.
ul. Marynarska 15
02-674 Warszawa
tel: +48 22 375 48 88
faks: +48 22 375 47 00
e-mail: kontakt.polska@novartis.com
z poważaniem,
Piotr Czerkies
Dyrektor Medyczny
ZAŁĄCZNIK 1: Wskazówki dotyczące reklamacji
Firma Novartis dokona reklamacji każdej zablokowanej ampułko-strzykawki z produktem leczniczym Leqvio. Aby dokonać reklamacji produktu, należy skontaktować się z:
Novartis Poland Sp. z o.o.
ul. Marynarska 15
02-674 Warszawa
tel: +48 22 375 48 88
faks: +48 22 375 47 00
e-mail: reklamacje.jakosciowe_pl@novartis.com